◆ Xeno FreeのヒトiPS細胞用培地
◆ マウスES/iPS細胞用培地
◆ ヒト・マウス神経幹細胞用培地
◆ ヒトMSC(間葉系幹細胞)用 Xeno Free培地
◆ ヒトES/iPS細胞培養システム
Cellartis DEF-CS 500 Culture System(製品コード Y30010)
- 培地と培地添加剤、プレートコーティング剤を含むオールインワンの培養システム
- フィーダーフリー培養条件下でシングルセルに分散した状態で継代が可能
- 長期間の未分化維持培養が可能であり、未分化細胞の選択が不要
-
未分化状態を維持した高効率なシングルセルクローニングにも最適


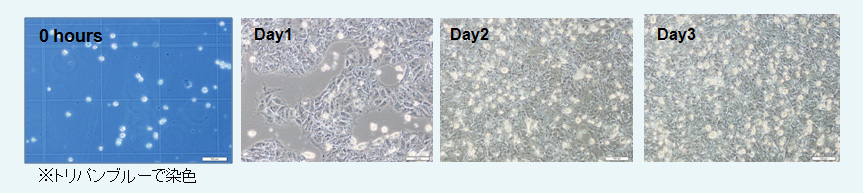
ヒトiPS細胞株(253G1)を本製品のプロトコールに従いシングルセルにまで分散し、トリパンブルーで染色した。
ほとんどの細胞が生細胞であることを確認後、本培地にて細胞を播種し培養を行った。
Cellartis DEF-CS 500 Culture Systemを用いた培養では、単一細胞に分散した状態で継代可能であった。
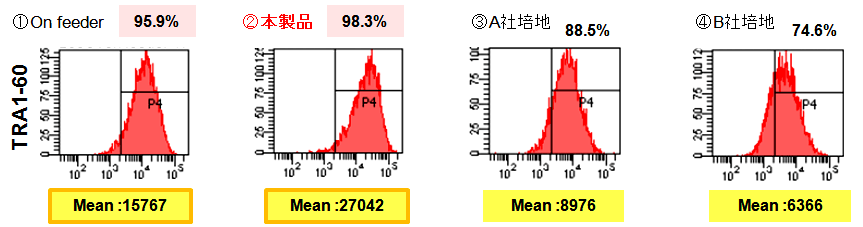
上記の培養条件① ~ ④でヒトiPS細胞株(253G1)を5週間培養後、細胞を回収して未分化マーカーTRA1-60の発現をフローサイトメトリーにて解析した。
Cellartis DEF-CS 500 Culture Systemで培養した細胞は高い陽性率と発現強度を示した。
◆ Xeno FreeのヒトiPS細胞用培地
Cellartis DEF-CS 500 Xeno-Free Culture Medium w/o antibiotics(製品コード Y30045)
- 動物・ヒト由来成分不含(Xeno-Free)
- シングルセルでの継代が可能
- 未分化状態での長期間の継代が可能(多機能性、自己再生、分化能のポテンシャルを長期間維持)
- 前臨床での使用に最適
- ロット間差が少なく安定したiPS細胞培養が可能
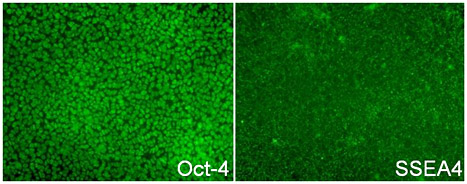
未分化状態での長期間の培養が可能
本製品を用いてヒトiPS細胞の継代を10回行った後、未分化能の状態が維持されていることを未分化マーカーOct-4とSSEA4に対する免疫染色で確認した。プレートコーティング剤はCorning Synthemax II-SC Substrate(Corning社, Cat. No. 3535)を使用
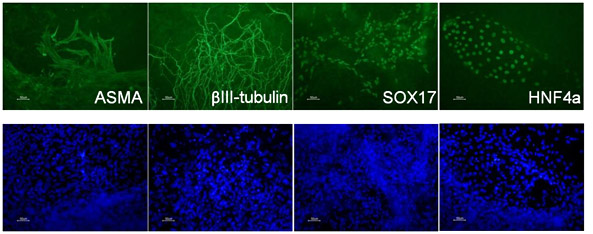
長期間継代後も多分化能を維持
本製品を用いてヒトiPS細胞の継代を10回行った後、三胚葉への分化能が維持されていることを各胚葉特異的抗体での免疫染色(中胚葉ではASMA、外胚葉ではβIII-tubulin、内胚葉ではSOX17、HNF4aを検出)で確認した。下図の核染色はDAPIを使用。培養時のプレートコーティング剤はCorning Synthemax II-SC Substrate(Corning社, Cat. No. 3535)を使用
研究用ヒトES/iPS細胞用培地 StemFit AK02N(製品コード AK02N)
- 多能性幹細胞を未分化状態で培養可能な研究用培地
- 簡便、安定に細胞増殖が可能
- 動物由来成分不含(ヒト由来成分は含有)
- フィーダーフリー条件下で培養が可能
- iPS細胞のクローニングが可能
- 外胚葉、中胚葉、内胚葉への分化が可能
- 多様な足場材での培養が可能

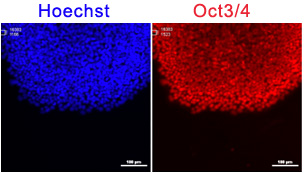
ヒトiPS細胞の未分化マーカーの発現
ヒトiPS細胞株(201B7)を本製品で、3継代の培養を行った後(28日目)、未分化マーカーOct3/4の発現を免疫染色で解析した。プレートコーティング剤はiMatrix-511(製品コード 892011)を使用。
◆ マウスES/iPS細胞用培地
Cellartis 3i mES/iPSC Culture Medium(製品コード Y40011)
- 無血清、フィーダーフリー、サイトカイン無添加の条件下で“Ground State”を維持したままマウスES細胞の培養が可能
- 難樹立マウス種からのES細胞株の樹立時にも使用可能
- C57BL/6NマウスでのGerm-line transmission効率が良好
- 分化誘導シグナルを抑え、刺激性サイトカイン無しに多能性を維持しながら増殖させる働きをもつ3種類の低分子阻害剤を含有
- Cellartis 3i mES/iPSC Culture Mediumで培養したマウスES細胞は、LIF、BMPの存在下での培養と同程度の倍加時間で増殖を続け、さらに、より高い多能性クローン形成能を示す。
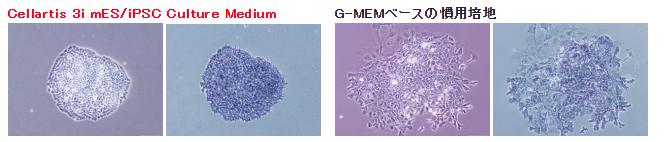
【未分化状態の確認】
Cellartis 3i mES/iPSC Culture Medium、または慣用培地で培養したマウスES細胞E14Tg2A株(左)とアルカリホスファターゼ染色画像(右)
Cellartis 3i mES/iPSC Culture Mediumで培養した細胞は、ムラのない染色像から均一な未分化細胞であることが分かる。 (弊社比較データ)

Cellartis 3i mES/iPSC Culture Mediumで培養したES細胞による高いキメラマウス作製率
ジーンターゲティングを目的として、Cellartis 3i mES/iPSC Culture Medium+LIFおよびA社培地+LIFで10継代培養したマウスES細胞(C57BL/6Nマウス由来)を8細胞期胚(CD1(ICR))にインジェクションし、翌日移植して生まれてくるマウス個体の毛色にてキメラ率を検証した。
その結果、Cellartis 3i mES/iPSC Culture Mediumを使用した場合、マウスは全てC57BL/6N由来の黒い毛色であり、キメラ率が良好であることが確認できた。
本データは、東京大学 国際高等研究所 ニューロインテリジェンス国際研究機構
鵜飼 英樹 先生よりご提供いただきました。
2iによるGround State維持
Cellartis 2i mES/iPSC Culture Medium(製品コード Y40031)
- フィーダー細胞不要、血清やLIF添加なしで、ground stateを維持したまま、マウスES細胞の培養が可能
- 2種類の低分子阻害剤(CHIR99021, PD0325901=‘2i’)存在下でマウスES細胞株、iPS細胞株を作製するために調製された化学的成分既知の無血清培地
- 2種類の低分子阻害剤はそれぞれ、GSK3β、またはERK / MEKからの分化誘導シグナルを抑制する効果を持ち、細胞の生存を促進する。
- 2i 阻害剤は、生殖系列に分化可能なES細胞を得ることが困難であったマウス種からの誘導や、ヒトおよび 家畜iPS細胞を作製する目的にも使用されている。
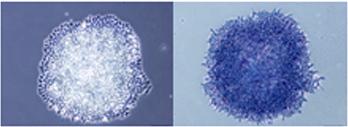
ES細胞E14Tg2A株
(右) アルカリホスファターゼ染色
◆ ヒト・マウス神経幹細胞用培地
マウスES細胞の神経分化に NDiff 227(製品コード Y40002)
- NDiff 227培地のみでマウスES細胞を神経細胞へ分化させることが可能
- 添加因子を加えることにより、マウスES細胞の無血清、フィーダー細胞非存在下での培養にも使用可能
- 増殖因子を添加することにより、ヒトES細胞の培養や、ground state でのヒトiPS細胞培養にも利用可能
- FGFを添加することにより、 NDiff 227培地はマウスES細胞から、肝臓や膵臓へ分化できるADE(Anterior Definitive Endoderm)前駆体を生じることも可能
- NANOGおよびKLF2をヒトの多能性幹細胞に過剰に発現させ、 NDiff 227培地を利用して培養すると、 約10~14日で平坦な形状をとるプライム型の多能性幹細胞からナイーブ型のドーム状のコロニーへと 変化する報告もある。
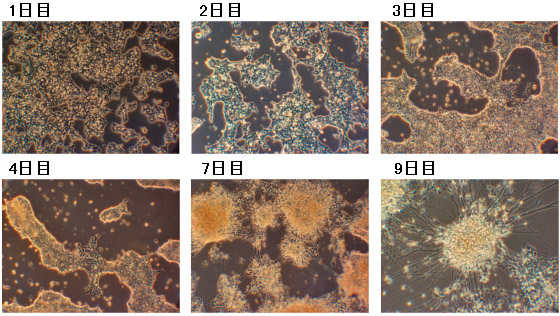
マウス・ヒト神経幹細胞の維持や神経分化に RHB-A(製品コード Y40001)
- EGFやFGF-2を添加して使用することで、無血清で接着培養状態の神経幹細胞の維持や拡大培養に使用可能
- 増殖因子を加えずに本培地で神経幹細胞を接着培養すると、神経細胞に機能的に分化することが可能
- in vitroでのヒト脳の器官初代培養において、放射状グリア由来の神経幹細胞の拡大培養や分化にも使用可能
- フィーダーフリーの継代数の低いES細胞を0.5~2×104 cells/cm2の密度でゼラチンコートのプレートにRHB-A培地を用いて播種する。
- 1~2日ごとに培地を交換する。神経細胞への分化の初期段階でかなりの数の死細胞が観察される。
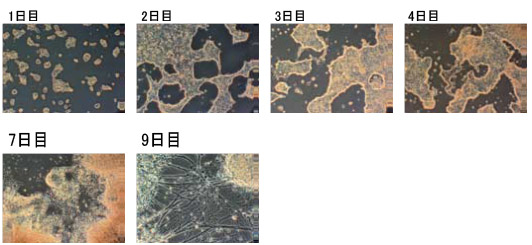
- 神経細胞への分化を形態観察、またマーカーの発現などで観察する神経細胞への分化は、4~6日目から観察され、7~9日目にニューロン成熟が見られる。
◆ ヒトMSC(間葉系幹細胞)用 Xeno-Free培地
Cellartis MSC Xeno-Free Culture Medium(製品コード Y50200)
- 動物由来成分を含まないXeno-Free培地であり、細菌やウイルスの感染リスクを低減
- タンパク質由来のコーティング剤を使用せずに、効率的かつ安定的(優れた細胞増殖と未分化維持)に培養でき、製造プロセスの単純化やコスト削減が可能
培養条件
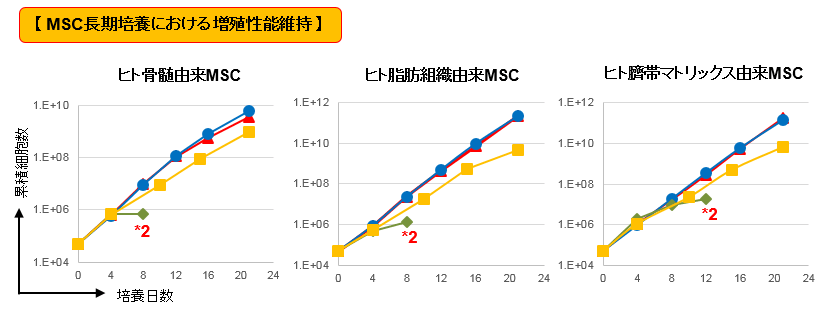
ヒト骨髄、脂肪、臍帯マトリックス由来の3種のMSCのそれぞれについて、Cellartis MSC Xeno-Free Culture Medium(本培地)、および、A社Xeno-Free培地(A社XF培地)を用いて、コーティング剤 有(コート剤 有)/無(コート剤 無)の2条件で3週間(21日間)培養した。また、いずれのMSCも、4.0×104 cells/well(培地はそれぞれ2 ml、6-wellプレート使用)で培養を開始した。
*1 「コート剤 有」の場合は、ヒト血漿由来フィブロネクチン溶液を用いてコーティングした培養容器を使用した。
*2 A社Xeno-Free培地(コート剤 無)については、各MSCの培養容器への大幅な接着率低下が確認された時点で培養を中断した。
- ▶ Cellartis MSC Xeno-Free Culture Mediumで培養したMSCは、優れた増殖性を示した。また、「コーティング剤 無」でもほぼ同等の増殖性能であることが分かった。
- ▶ A社Xeno-Free培地を用いて「コーティング剤 無」で培養した全てのMSCは、2継代目以降に培養容器への接着率の大幅な低下が確認された(*2)。
