
ウイルス安全性評価試験
タカラバイオ株式会社は、弊社の完全子会社であるViSpot株式会社の吸収合併を完了し、ウイルス安全性評価試験受託サービスを弊社のCDMOサービスに組み込み、 再生医療等製品/バイオ医薬品の開発・製造・品質試験に関するワンストップサービスをより強化しました。国内で試験実施を行うことによって、ご希望納期やカスタムのご相談について、これまで以上にきめ細やかに対応できるようになりました。




お客様の時間、利便性、リソースを大切にします。
■ViSpotの受託サービス
ウイルスクリアランス試験
ウイルス試験 (バイオ医薬品安全性試験)
ViSpot沿革
| 2016年 | MAB組合プロジェクトとしてウイルス安全性管理技術が採択(神戸大学で研究開始) |
| 2017年09月 | ViSpot株式会社設立 |
| 2018年04月 | MAB組合の第2期にViSpotとして参画 |
| 2019年01月 | ウイルスクリアランス試験(non-GLP)の受託開始 |
| 2019年07月 | GLP準拠の品質管理体制を構築 |
| 2020年01月 | ウイルスクリアランス試験(GLP準拠試験)の受託開始 |
| 2020年10月 | 抗ウイルス活性評価試験の受託開始 |
| 2021年10月 | GMP準拠の品質管理体制を構築 |
| ウイルス試験(GMP体制下の品質試験) | |
| 2022年11月 | 試験室の増床(神戸ラボ) |
| 2024年01月 | 試験施設新設(ウイルス試験・六甲ラボ)、試験実施準備開始 |
| 2024年08月 | 六甲ラボ稼働開始 |
| 2025年03月 | タカラバイオ株式会社完全子会社化 |
| 2025年05月 | タカラバイオ株式会社吸収合併ViSpot事業本部体制 |
ウイルス安全性評価試験 ~バイオ医薬品の重要なサプライチェーンのピース~
ウイルス安全性評価試験は、バイオ医薬品等の安全性を担保するために、原材料、製造工程、 製品の各ステップにおいて、ウイルス存在の有無を評価するバリデートされた各種試験を指します。 ウイルス安全性評価試験は、ウイルスクリアランス試験とウイルス試験とから成り立っています。
| 医薬品等のウイルス安全性保証の3ステップ | ||
| 原材料 | 製造工程 | 製品 |
| ウイルス試験 2021年~ <GMP体制> |
ウイルスクリアランス試験 2019年~ <GLP体制> |
ウイルス試験 2021年~ <GMP体制> |
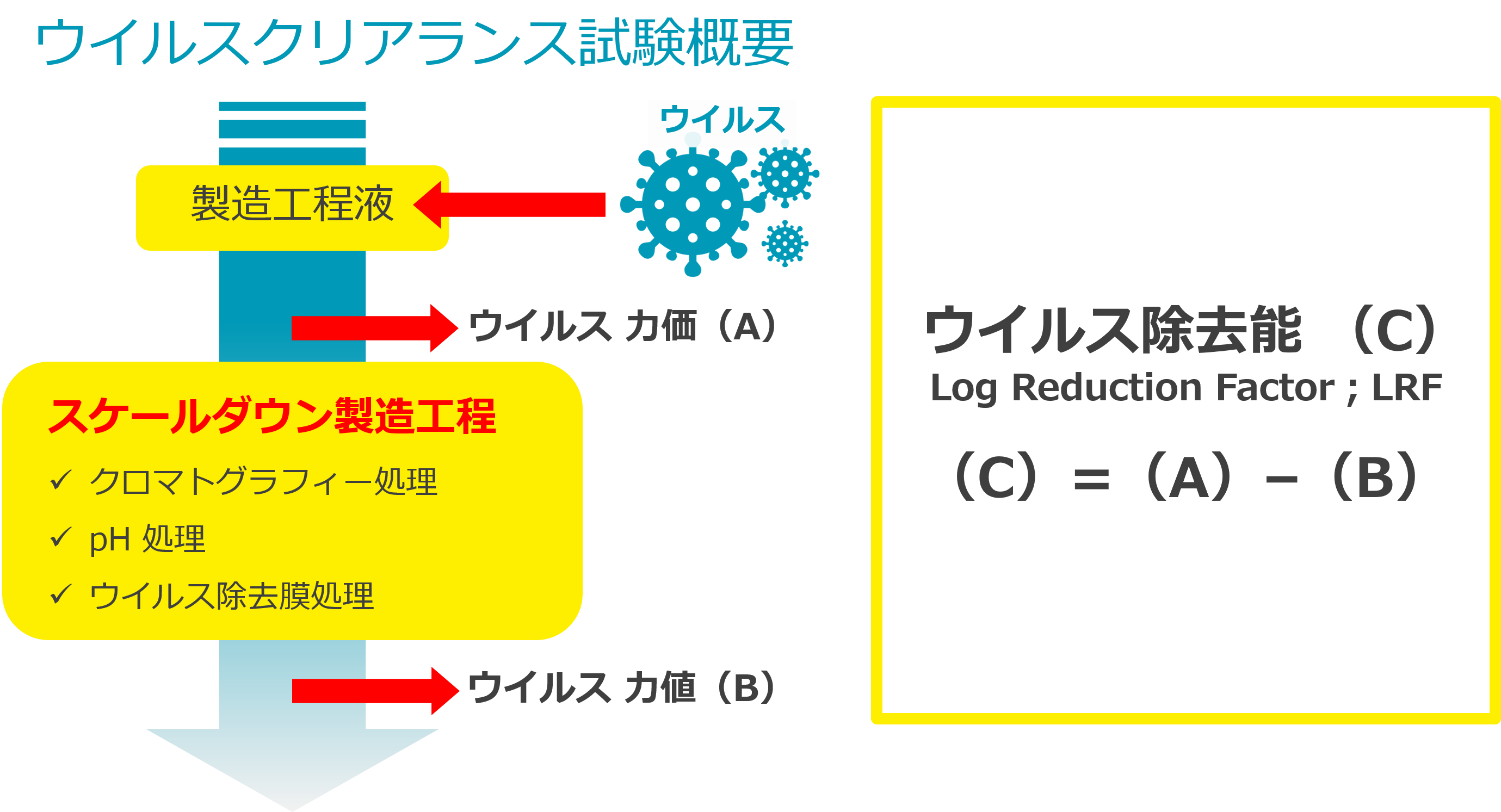
ウイルスクリアランス試験
対象とする製造工程がウイルスを除去・不活化する能力を有するかどうかを、製造工程のスケールダウンモデルにウイルスをスパイクするチャレンジ試験で検証します。

ウイルス試験(バイオ医薬品安全性試験)
対象となる被験試料(細胞や培養液など)におけるウイルス存在の有無をいくつかの異なる手法で検出します。
ViSpot提供 ウイルス試験項目
| 試験分類 | 試験法 | 試験内容 |
| レトロウイルス および 内在性ウイルス試験 |
レトロウイルス感染性試験 |
|
| 透過型電子顕微鏡 (TEM) |
|
|
| 逆転写酵素活性 (Q-PERT) |
|
|
| 非内在性ウイルス または 外来性ウイルス試験 |
in vitro ウイルス試験 |
|
| in vivo 試験 |
|
|
| 抗体産生試験 |
|
|
| ウシまたはブタウイルス試験* |
|
|
| 特定ウイルスのNAT(PCR) |
|
|
| その他 | 無菌試験(微生物限度試験) |
|
| マイコプラズマ試験 |
|
|
| エンドトキシン試験 |
|
* 2026年春頃再リリース予定
その他の品質試験サービスはこちら
